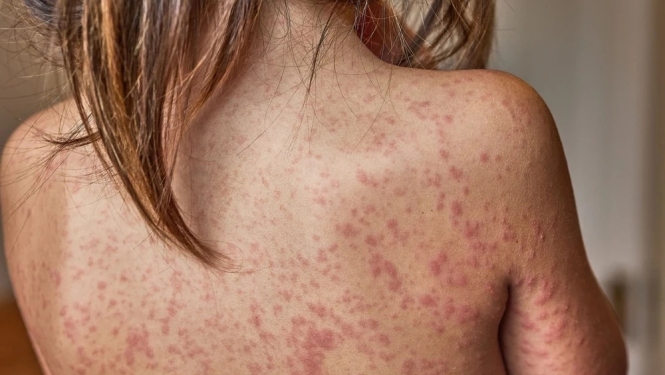
Slimību profilakses un kontroles centrs (SPKC) informē, ka Latvijā turpinās masalu izplatīšanās – līdz 2026. gada 7. aprīlim reģistrēti 42 saslimušie. Saslimšanas gadījumi konstatēti dažādās vecuma grupās, tostarp 29 bērniem, no kuriem neviens nebija vakcinēts pret masalām. Plašāka informācija par saslimušo skaitu pieejama SPKC tīmekļvietnē. SPKC ir vērsies pie ģimenes ārstiem, nosūtot ģimenes ārstu asociācijām detalizētu informāciju par vakcinācijas aptveri pret masalām, aicinot aktīvi uzrunāt…
Slimību profilakses un kontroles centrs (SPKC) informē, ka Latvijā turpinās masalu izplatīšanās – līdz 2026. gada 7. aprīlim reģistrēti 42 saslimušie. Saslimšanas gadījumi konstatēti dažādās vecuma grupās, tostarp 29 bērniem, no kuriem neviens nebija vakcinēts pret masalām. Plašāka informācija par saslimušo skaitu pieejama SPKC tīmekļvietnē. SPKC ir vērsies pie ģimenes ārstiem, nosūtot ģimenes ārstu asociācijām detalizētu informāciju par vakcinācijas aptveri pret masalām, aicinot aktīvi uzrunāt nevakcinētos pacientus. Padziļinātas E‑veselības sistēmā reģistrēto vakcinācijas datu analīzes rezultātā SPKC konstatēja nepietiekamu vakcinācijas aptveri. Analizētajās vecuma grupās (16–36 mēneši, 8–9 gadi) reģistrēti 50 645 bērni, no kuriem tikai…